近日,华中科技大学武汉光电国家研究中心与澳大利亚Adelaide大学ARC杰出纳米级生物光子学中心合作,通过活体光学显微成像揭示坐骨神经损伤诱导的小胶质细胞活化状态的动态改变,以及疼痛程度与小胶质细胞特征参数(如细胞密度、形态、突起长度和运动速度)变化之间的关系。相关研究成果以“Graded peripheral nerve injury creates mechanical allodynia proportional to the progression and severity of microglial activity within the spinal cord of male mice”为题发表在《Brain Behavior and Immunity》上。
神经损伤造成的脊髓小胶质细胞活化与神经病理性疼痛的发展及持续性密切相关。该研究通过对慢性束缚性损伤小鼠脊髓中的小胶质细胞进行长达14天的活体显微成像,监测小胶质细胞在此过程中细胞的密度、形态及运动等特征参数,同时结合对小鼠机械性痛觉程度的检测,发现小胶质细胞的活化状态与痛觉超敏的等级呈正相关。另外,通过对疼痛小鼠的躯体感觉皮层中血氧饱和度动态变化的观察,直观展示了疼痛刺激一侧的神经元活动增加。最后,通过对成像观察到的小胶质细胞状态进行定量分析,在一定程度上解释了在外周损伤后小胶质细胞诱发快速且持续性脊髓背角功能性改变的原因。
1、 不同等级神经病理性疼痛发展过程中小胶质细胞活性状态的改变
按照如图1所示的实验设计,对小鼠进行脊髓窗安装和神经束缚性损伤造模,并在对应时间点进行疼痛行为的监测以及脊髓的活体显微成像。
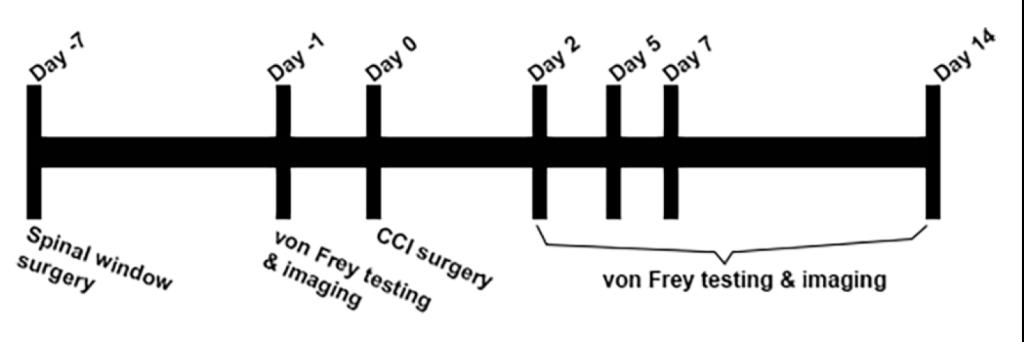
Fig. 1 Timeline for intravital imaging of spinal cord
该研究通过对小胶质细胞的密度、形态、突起长度及运动等特征参数的监测来表征小胶质细胞的活化状态(图2)。经过长达14天的活体动态监测,并分析疼痛损伤前后脊髓小胶质细胞的特征参数,结果显示,在损伤发生前,不同组别的小胶质细胞的各参数基本一致。随着疼痛的发展,从损伤后的第7天到第14天,刺激侧小胶质细胞的密度明显增加,且这种增加与疼痛损伤程度的加剧呈正相关。接着他们发现在刺激同侧中,从损伤后的第2天到第14天,小胶质细胞的形态由静息状态下的分支状转变为活化状态下的变形虫样,从第5天至第14天,细胞的形态变化与疼痛程度呈正相关。小胶质细胞的突起运动变化,在损伤后的第7天至第14天,突起的运动速度由快至慢,且与神经疼痛的加剧呈负相关。综上所述,随着神经病理性疼痛进程的发展,在刺激同侧的脊髓,小胶质细胞的密度增加、细胞变大、细胞突起的运动减缓,这些变化均与疼痛程度的增加密切相关。
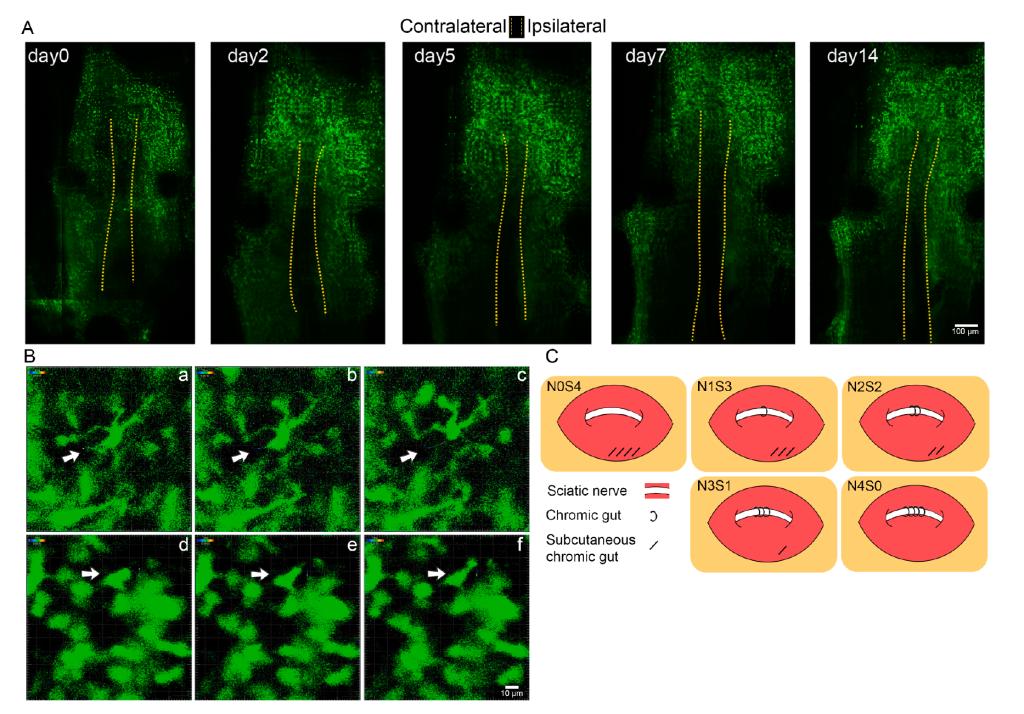
Fig. 2 Intravital spinal cord images of microglia from the
contralateral and ipsilateral dorsal spinal cord
2、 躯体感觉皮层神经元活动变化
对疼痛小鼠躯体感觉皮层S1HL区光声信号(PA)进行成像监测,与对照组N0S4小鼠相比,PA值无论在刺激侧还是对侧都有显著性的升高(图3)。这说明,在疼痛小鼠皮层中血红蛋白的含量更高。通过对氧合血红蛋白光声信号的分析可见,在疼痛小鼠中刺激对侧的血氧饱和度比同侧更高。此结果提示坐骨神经损伤后可导致对侧脑区的血氧饱和度和神经元活动增加。
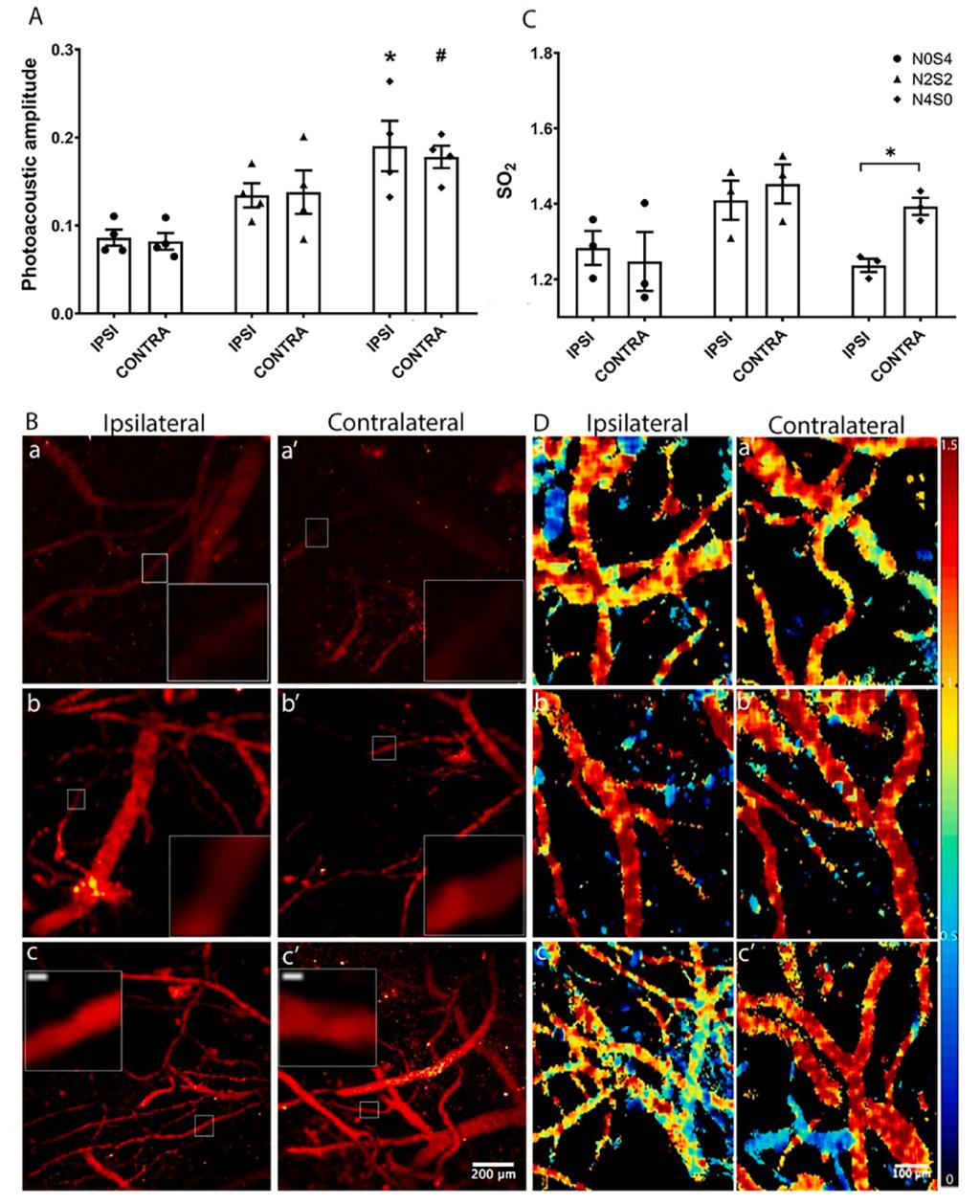
Fig. 3 Photoacoustic amplitude (PA) and oxygen saturation (SO2)
alteration in S1HL regions from different graded pain mice
该研究通过使用不同等级的神经束缚性损伤动物模型并结合活体显微荧光成像及光声显微成像,对神经病理性疼痛发展过程中的小鼠脊髓小胶质细胞及躯体感觉皮层血氧饱和度变化进行监测。研究发现:1)损伤后的第14天,小胶质细胞的密度增大、形态变大、突起速度减慢,活性状态发生明显的改变,已从静息状态转变为激活状态;2)疼痛小鼠的躯体感觉皮层血氧饱和度更高,显示神经元活动增加;3)小胶质细胞活化状态的改变与疼痛刺激程度及小鼠神经病理性疼痛行为成正相关。这些结果提示,控制小胶质细胞的过度活化,有可能减缓神经损伤及慢性疼痛的程度,成为一种潜在的新型治疗策略。
该研究得到国家杰出青年科学基金(81625012)、国家自然科学基金(61721092)、华中科技大学学术前沿青年团队项目和武汉光电国家研究中心创新基金以及澳大利亚ARC杰出纳米级生物光子学中心(CE140100003)的资助。本实验室张智红教授为文章的通讯作者,澳大利亚Adelaide大学ARC杰出纳米级生物光子学中心Vasiliki Staikopoulos和本实验室乔莎博士为文章共同第一作者。
论文全文下载地址:
https://www.sciencedirect.com/science/article/pii/S0889159120323941