近日,《ACS Nano》杂志在线发表了华中科技大学武汉光电国家研究中心生物医学光子学研究部、华中科技大学生物医学光子学教育部重点实验室张玉慧教授课题组与合作团队武汉血液中心马严课题组的研究论文《Surface-Functionalized Halo-Tag Gold Nanoprobes for Live-Cell Long-Term Super-Resolution Imaging of Endoplasmic Reticulum Dynamics》。该研究通过在金纳米颗粒表面修饰荧光基团Atto565,靶向基团Halo-tag以及细胞穿膜肽fR8,克服了金纳米颗粒容易困在囊泡中的挑战,构建了具有高亮度、高光稳定性和高生物相容性的金纳米荧光探针(GNP-Atto565-fR8-CA),实现了对内质网动态变化过程的超分辨长时程成像,为探索活细胞内质网的超微结构和动力学提供了实用的工具。
内质网作为真核细胞中的关键细胞器,在蛋白质的合成、加工及修饰等过程中扮演着核心角色。其功能的紊乱与癌症、炎症、代谢失调及神经退行性疾病等多种严重疾病密切相关。因此,深入探索内质网的动态变化过程,对于揭示这些疾病的发病机制至关重要。近年来,超分辨率成像已成为研究细胞结构及其动态过程的有力工具,极大地增强了我们对细胞生物学的认识。然而,缺乏高亮度,高光稳定性和稳定的标记探针使得ER的长时程超分辨成像仍然具有挑战性。
为解决上述问题,张玉慧教授团队设计并制备了一种新型表面功能化Halo-tag金纳米荧光探针(GNP-Atto565-fR8-CA)。如图1所示,该探针以聚乙二醇(PEG)修饰的3.5纳米金纳米颗粒为核心,结合了荧光染料Atto565、细胞穿透肽fR8和Halo-tag配体氯代烷烃(CA)。这一设计实现了多重优势:金纳米颗粒作为平台,同时负载多个Atto565染料分子,从而显著增强了探针的荧光亮度;细胞穿透肽fR8的引入使得探针能够高效进入细胞质,克服了金纳米颗粒容易困在囊泡中的挑战;而Halo-tag技术的引入,是通过构建稳固的共价键,实现了对内质网蛋白的高精度、高特异性标记,为后续的生物学研究奠定了坚实基础。综上所述,这一设计不仅提升了探针的荧光性能与光稳定性,还巧妙地解决了金纳米颗粒在细胞内的递送难题,实现了对内质网的精准靶向与长时程成像。
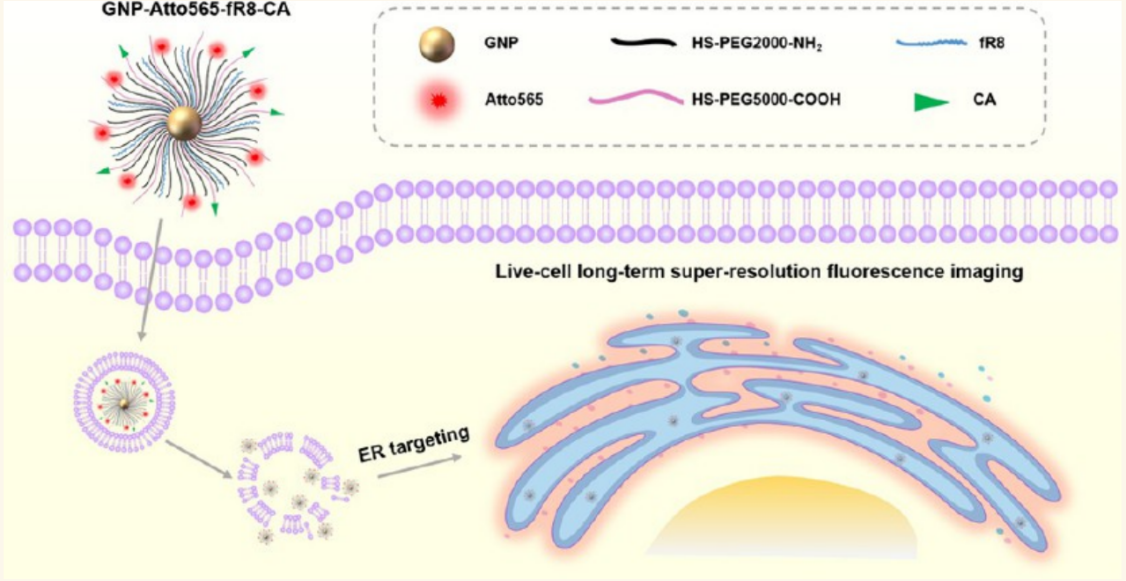
图1. GNP-Atto565-fR8-CA金纳米探针标记内质网示意图
实验结果显示,GNP-Atto565-fR8-CA探针除了具有较好的胞质递送效果以及ER靶向特异性,还表现出优异的荧光亮度和光稳定性。与当前广泛使用的商业有机荧光探针相比,该探针在亮度上提升了约四倍,光稳定性提高了三倍,并能够在动态活细胞超分辨率成像中稳定记录高达1000帧的图像。基于GNP-Atto565-fR8-CA探针具有高亮度、高光稳定性、高特异性、高标记稳定性、高生物相容性等优势,研究团队利用SIM超分辨成像系统跟踪并观察到了内质网的长期动态过程,包括内质网小管的伸长、收缩、融合等;同时,还捕获了内质网与线粒体(内质网-线粒体接触位点处线粒体的分裂)和溶酶体(内质网与溶酶体之间的“搭便车”行为)的相互作用过程(图2)。
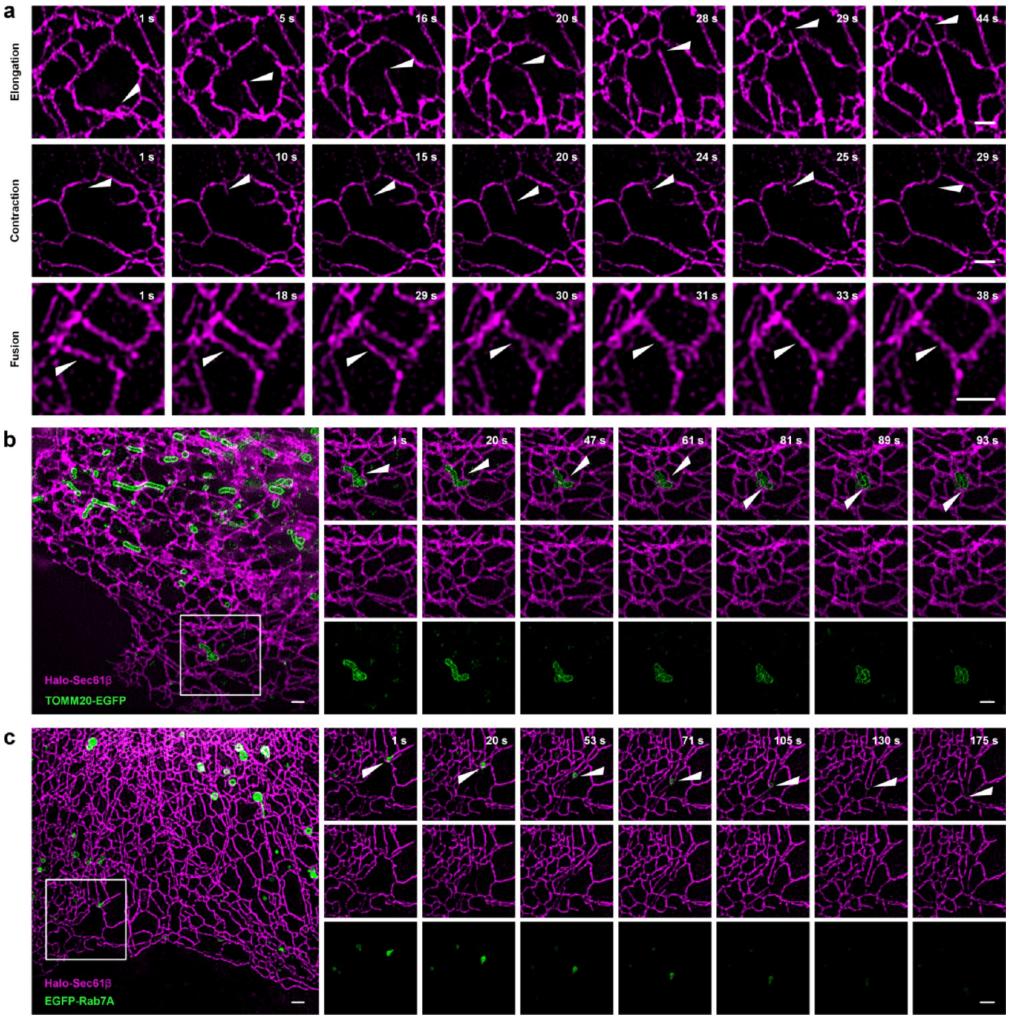
图2 活细胞内质网动态长时程SIM成像结果
华中科技大学武汉光电国家研究中心生物医学光子学研究部张玉慧教授和武汉血液中心马严博士为共同通讯作者。武汉市第四医院副研究员徐彭(原张玉慧教授课题组博士后)和张玉慧教授课题组博士生钟思梅为共同第一作者。华中科技大学武汉光电国家研究中心生物医学光子学研究部博士生魏云飞、段欣欣、博士后张朦及武汉市第四医院神经内科沈伟教授为共同作者。
该项目得到国家重点研发计划(2022YFC3401100)、国家自然科学基金(92354305、32271428、32201132)、中国博士后科学基金(BX20220125、2022M711257)、湖北省卫生厅项目(BX20220125、2022M711257)、湖北省卫生计生科研基金(WJ2023M138)和武汉光电国家研究中心主任基金的支持。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.4c06138